Der Bluthochdruckschalter in der Nebenniere
Jülich, 20. Februar 2018 – Ein internationales Team von Wissenschaftlerinnen und Wissenschaftlern hat die Mechanismen einer Form des Bluthochdrucks aufgeklärt. Jülicher Forscher konnten dabei erstmals zeigen, wie ein bestimmtes Protein den Unterschied zwischen den Chloridkonzentrationen innerhalb und außerhalb der Zelle benutzt, um den Blutdruck zu regulieren. "Biologische Informationsverarbeitung findet nicht nur in Nervenzellen und im Gehirn, sondern in jeder Zelle unseres Körpers statt", erklärt Prof. Christoph Fahlke von Jülicher Institute of Complex Systems. "Es gibt eine Vielfalt von Mechanismen, mit denen Zellen externe Signale aufnehmen und verarbeiten können."
Mehr als eine Milliarde Menschen weltweit leiden an Bluthochdruck, in Industrieländern wie Deutschland sind etwa 30 Prozent aller Erwachsenen davon betroffen. Längerer Bluthochdruck schädigt die Gefäße, was zu Durchblutungsstörungen führen kann: Mögliche Folgen sind Herzinfarkt, Nierenversagen, Schlaganfall. Die Ursachen für Bluthochdruck sind vielfältig. Neben bekannten Risikofaktoren wie Übergewicht, Salz- und Alkoholkonsum spielen auch genetische Ursachen eine Rolle. Schon eine Mutation eines einzelnen Gens kann zur familären Hypertonie führen, einer erblichen Veranlagung für Bluthochdruck, die schon bei Kindern und Jugendlichen auftreten kann.
Etwa ein Prozent aller Arten von Bluthochdruck wird durch eine Überproduktion des Hormons Aldosteron verursacht. Dieses wird in der Nebennierenrinde gebildet und reguliert unseren Salz- und Flüssigkeitshaushalt. Die Ursache der Überproduktion von Aldosteron sind oft Funktionsveränderungen von einzelnen Proteinen, die in der Signalverarbeitung von Zellen eine Rolle spielen.
Durch die Aufklärung des Genoms verschiedener Testpersonen und ihrer Familien konnte ein Team um Ute Scholl von der Charité in Berlin und Richard Lifton vom Laboratory of Human Genetics und Genomics der Rockefeller University in New York eine Ursache der Aldosteron-Überproduktion identifizieren: Mutationen in CIC-2, einem Ionenkanal-Protein, welches Chlorid-Ionen das Durchqueren von Zellmembranen ermöglicht.
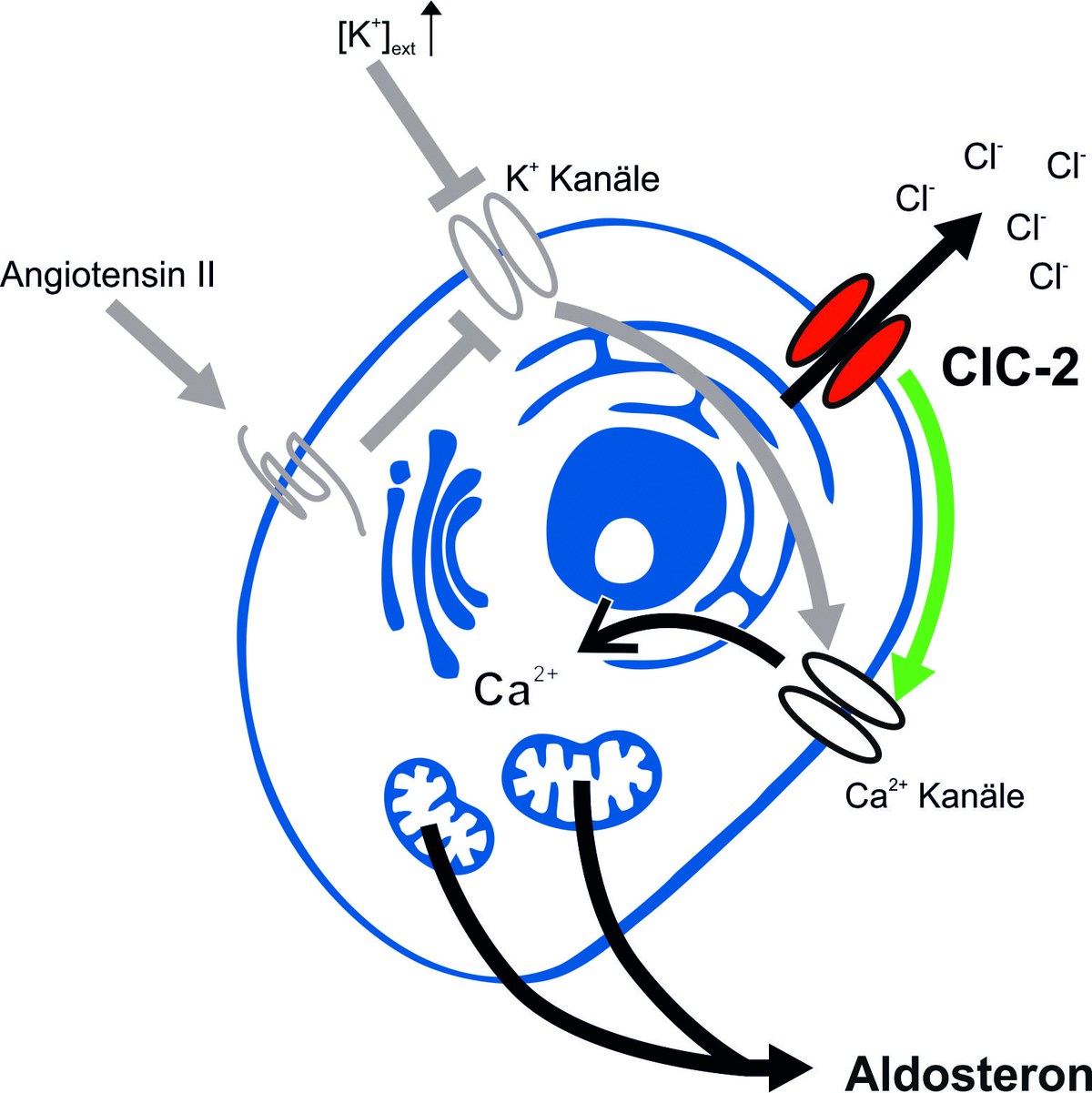
Wie diese Mutationen die Funktion von CIC-2-Kanälen und der Nebennierenrinde von Patienten beeinträchtigen, hat die Arbeitsgruppe von Christoph Fahlke aufgeklärt. Die Wissenschaftler konnten zeigen, dass in den Aldosteron-produzierenden Zellen eine sehr hohe Konzentration von Chlorid-Ionen existiert. Dies führt dazu, dass die Aktivierung von ClC-2 die Zellen erregt und zur Synthese von Aldosteron antreibt. Die genetischen Veränderungen in den CIC-2-Kanälen von bestimmten Patienten führen dazu, dass diese elektrische Zellanregung auch schon bei geringeren Reizen stattfindet: Es kommt zur Aldosteron-Überproduktion.
Mit diesen neuen Erkenntnissen konnte so zum ersten Mal die Bedeutung von CIC-2-Proteins für die Signalverarbeitung innerhalb von Zellen verstanden werden. Neben der Aufklärung der Rolle von ClC-2 für den Krankheitsmechanismus und die Funktion der Nebenniere gibt die neue Veröffentlichung auch noch weitere Impulse für die Forschung der nächsten Jahre. "Abgesehen von einigen Ausnahmen ist die Bedeutung von Anionen wie Chlorid in der Verarbeitung von Informationen innerhalb der Zelle bislang eher stiefmütterlich behandelt worden", so Christoph Fahlke. "Mit der Vielzahl verfügbarer Techniken und erfahrener Wissenschaftler sind wir in einer hervorragenden Lage, diese Wissenslücke in der Zukunft weiter zu schließen."
Originalpublikation: CLCN2 chloride channel mutations in familial hyperaldosteronism type II,
Ute I. Scholl, Gabriel Stölting, Julia Schewe, Anne Thiel, Hua Tan, Carol Nelson-Williams, Alfred A. Vichot, Sheng Chih Jin, Erin Loring, Verena Untiet, Taekyeong Yoo, Jungmin Choi, Shengxin Xu, Aihua Wu, Marieluise Kirchner, Philipp Mertins, Lars C. Rump, Ali Mirza Onder, Cory Gamble, Daniel McKenney, Robert W. Lash, Deborah P. Jones, Gary Chune, Priscila Gagliardi, Murim Choi, Richard Gordon, Michael Stowasser, Christoph Fahlke and Richard P. Lifton,
Nature Genetics, DOI: 10.1038/s41588-018-0048-5
Weitere Informationen:
Institute of Complex Systems, Zelluläre Biophysik (ICS-4)
Forschungszentrum Jülich
Ansprechpartner:
Prof. Christoph Fahlke
Institute of Complex Systems, Zelluläre Biophysik (ICS-4)
Forschungszentrum Jülich
Tel.: 02461 61-3016
E-Mail: c.fahlke@fz-juelich.de
Pressekontakt:
Annette Stettien
Unternehmenskommunikation, Forschungszentrum Jülich
Tel. +49 2461 61-2388
E-Mail: a.stettien@fz-juelich.de
Dr. Regine Panknin
Unternehmenskommunikation
Forschungszentrum Jülich
Tel.: 02461 61-9054
E-Mail: r.panknin@fz-juelich.de
